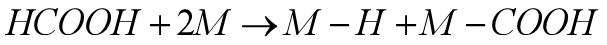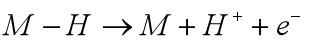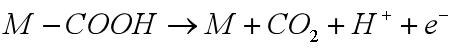1、技術簡介
電催化高級氧化技術是最近發(fā)展起來的處理有毒難生化降解污染物的新型有效技術,它通過陽極反應直接降解有機物,或通過陽極反應產生羥基自由基(·OH)、臭氧一類的氧化劑降解有機物,這種降解途徑使有機物分解更加徹底,不易產生毒害中間產物,更符合環(huán)境保護的要求,這種方法通常被稱為有機物的電催化氧化過程。所謂的電催化,是指在電場作用下,存在于電極表面或溶液相中的修飾物能促進或抑制在電極上發(fā)生的電子轉移反應,而電極表面或溶液相中的修飾物本身并不發(fā)生變化的一類化學作用。
2、基本原理
電化學技術的基本原理是使污染物在電極上發(fā)生直接電化學反應或利用電極表面產生的強氧化性活性物種使污染物發(fā)生氧化還原轉變,后者被稱為間接電化學轉化,見下圖:
原理圖
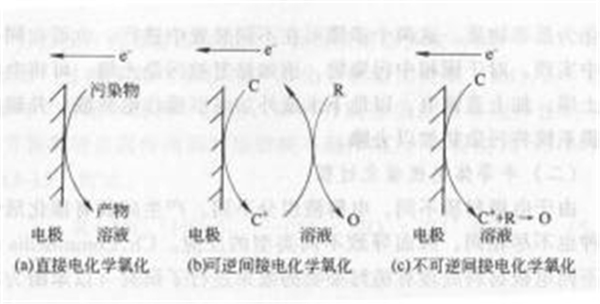
直接電化學轉化通過陽極氧化可使有機污染物和部分無機污染物轉化為無害物質,陰極還原則可從水中去除重金屬離子。這兩個過程同時伴生放出H2和O2的副反應,使電流效率降低,但通過電極材料的選擇和電位控制可加以防止,且很少產生羥基自由基,處理效率不理想。
間接氧化是通過陽極在高電勢下產生的羥基等自由基與污染物分子作用,這種自由基是具有高度活性的強氧化劑C(也可以是催化劑),通過對有機物產生脫氫、親電子和電子轉移作用,形成活化的有機自由基,產生連鎖自由基反應,使有機物迅速完全降解,故也稱為電化學燃燒。間接氧化在一定程度上既發(fā)揮了陽極直接氧化的作用,又利用了產生的氧化劑,使處理效率顯著提高。
3、電催化氧化技術降解有機物的機理
關于電催化氧化處理有機物的機理有很多種,其中被廣大研究者所接受的是由Comninellis Ch.提出的金屬氧化物的吸附羥基自由基和金屬過氧化物理論按照該理論。
有機物陽極氧化的一般過程如圖所示:
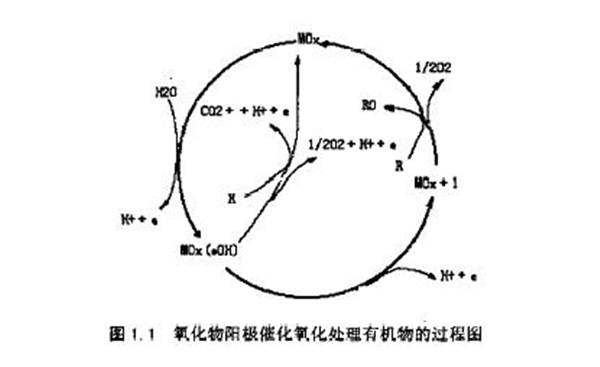
酸性(或堿性)溶液中的H2O(或OH-)在金屬氧化物陽極表面吸附,在表面電場的作用下,吸附的H2O(或OH-)失去電子,生成MOX(.OH) (MOx表示氧化物陽極):
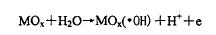
接下來,吸附的·OH可能與陽極材料中的氧原子相互作用,自由基中的氧原子通過某種途徑進入金屬氧化物MOx的晶格之中,從而形成所謂的金屬過氧化物MOx+1:
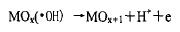
這樣在金屬的表面存在兩種狀態(tài)的“活性氧”:一種是物理吸附的活性氧,即吸附的羥基自由基,另一種是化學吸附的活性氧,即進入氧化晶格中的氧原子。當溶液中沒有有機物存在時,兩種活性氧都發(fā)生反應,生成氧氣。
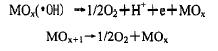
當溶液中有有機物存在時,物理吸附的氧(-OH)在“電化學燃燒”過程中起主要作用,而化學吸附的氧(MOx+I)則主要參與“電化學轉化”,即對有機物進行有選擇的氧化(對芳香類有機物起作用而對脂肪類有機物不起作用)。
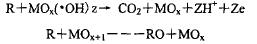
電催化反應的共同特點是反應過程包含兩個以上的連續(xù)步驟,且在電極表面上生成化學吸附中間物。許多由離子生成分子或使分子降解的重要電極反應均屬于此類反應。所以對電催化氧化(ECR)的機理主要是通過電極和催化材料的作用產生超氧自由基(·O2)、H2O2、羥基自由基(·OH)等活性集團來氧化水體中的有機物。
因此針對電催化反應的特點也可將此種反應分為兩類:
1)、離子或分子通過電子傳遞步驟在電極表面上產生化學吸附中間物,隨后吸附中間物經過異相化學步驟。或電化學脫附步驟生成穩(wěn)定的分子。如酸性溶液中的氫析出反應:
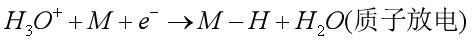
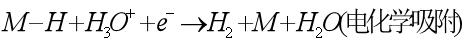
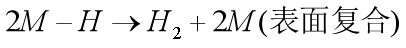
2)、反應物首先在電極上進行解離式(dissociative)或締合式(associative)化學吸附,隨后吸附中間物或吸附反應物進行電子傳遞或表面化學反應。如甲醛的電氧化: